生物技術產品與大分子藥物開發中的藥動學與藥效學考量 技術開發的核心因素
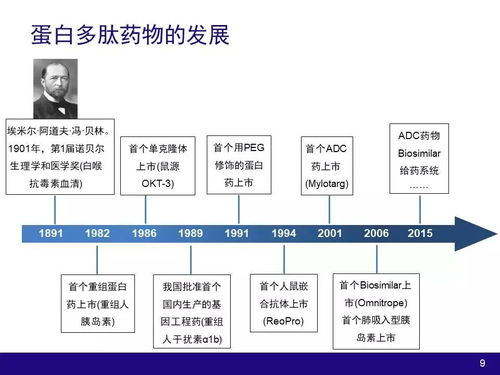
在當今藥物研發領域,生物技術產品與大分子物質(如單克隆抗體、重組蛋白、基因治療載體、疫苗等)已占據舉足輕重的地位。與傳統的化學小分子藥物相比,這些大分子藥物具有結構復雜、作用機制特異、靶向性強等優勢,但其開發過程也面臨著獨特的藥動學與藥效學挑戰。深刻理解并優化這些因素,是成功進行技術開發、將候選分子轉化為安全有效療法的關鍵。
一、 大分子藥物的獨特藥動學特性
大分子的藥動學行為與其物理化學性質密切相關,這些特性直接影響其體內過程,是技術開發中必須優先考慮的因素。
- 吸收:多數大分子藥物(如抗體、胰島素)因分子量大、親水性強,難以通過被動擴散透過生物膜。因此,口服給藥通常生物利用度極低,開發多采用注射途徑(靜脈、皮下、肌肉)。皮下注射的吸收依賴于淋巴系統,速率較慢且可能受注射部位、體積、制劑輔料影響。技術開發需重點優化給藥途徑和制劑處方,以提高吸收的可預測性和一致性。
- 分布:大分子藥物通常難以自由穿過血管內皮細胞間隙,分布容積較小,主要集中在血漿和細胞外液。其分布受分子大小、電荷、與血液成分結合以及靶點表達位置的影響。例如,抗體藥物需要穿透組織(如實體瘤)才能到達靶點,這常常是療效的限制因素。技術開發策略包括設計更小的抗體片段(如Fab、scFv)或使用增強組織穿透的遞送系統。
- 代謝與消除:小分子藥物主要經肝臟細胞色素P450酶代謝,而大分子藥物的消除途徑截然不同。其主要通過蛋白水解降解成小肽和氨基酸,或被網狀內皮系統(RES)吞噬清除。特異性消除途徑包括:
- 靶介導的藥物處置:藥物與高親和力、可飽和的靶點結合后內化并被降解。這是許多抗體藥物的主要消除途徑,導致其藥動學呈非線性(劑量依賴性)。
- 新生兒Fc受體循環:IgG抗體通過結合FcRn避免溶酶體降解,從而延長半衰期。這是抗體工程化延長半衰期的核心機制。
- 免疫原性:機體可能產生抗藥物抗體,加速藥物清除,甚至中和藥效或引發不良反應。這是技術開發中風險評估和緩解的重中之重。
二、 大分子藥物的藥效學核心與復雜性
大分子藥物的藥效學直接關聯其精巧的作用機制,但也因此更為復雜。
- 高特異性與靶點結合:大分子藥物通過精確的分子識別(如抗原-抗體、受體-配體)發揮作用。其藥效高度依賴于靶點的性質(密度、親和力、內化速率、信號傳導能力)和疾病狀態下的表達變化。技術開發需在早期進行深入的靶點驗證和表征。
- 作用機制的多樣性:機制遠比小分子藥物復雜,可能包括:阻斷信號通路(如抗TNF-α抗體)、介導細胞毒性(如ADCC、CDC)、遞送載荷(如抗體偶聯藥物ADC)、調節免疫系統(如免疫檢查點抑制劑)、或替代缺失蛋白(如凝血因子)。技術開發必須圍繞預期的藥效學作用來設計分子結構。
- 生物標志物與藥效動力學:由于作用直接,大分子藥物常伴有可測量的藥效動力學標志物(如受體占有率、細胞因子水平、腫瘤標志物變化)。這些標志物對于早期臨床開發中建立概念驗證、確定生物學有效劑量至關重要。
- 時間延遲效應:藥效的產生或消失可能滯后于血藥濃度的變化,這源于復雜的機制,如靶點合成/降解的動力學、下游信號傳導的級聯反應、或免疫系統的激活/抑制需要時間。這要求在建立PK/PD模型時考慮間接反應模型等復雜模型。
三、 技術開發中的綜合考量與策略
成功的生物技術產品開發,是貫穿始終的藥動學與藥效學整合優化過程。
- 臨床前研究設計:利用轉基因動物、人源化動物模型或疾病相關體外模型,早期評估候選分子的PK/PD特征,預測人體有效劑量和給藥方案。關注種屬差異,特別是靶點交叉反應性和免疫原性風險。
- 分子工程與優化:
- PK優化:通過定點突變增強FcRn結合以延長半衰期;聚乙二醇化或其他修飾減少腎臟清除;優化糖基化模式以調節效應器功能和半衰期。
- PD優化:通過親和力成熟增強靶點結合;工程化改造Fc段以增強或減弱ADCC/CDC效應;設計雙特異性抗體同時結合兩個靶點。
- 制劑與遞送技術開發:開發穩定的液體制劑或凍干制劑,防止聚集和降解。對于需要局部或靶向給藥的藥物(如眼科、吸入、腫瘤內注射),開發特殊的遞送系統以改善PK/PD特性。
- 臨床開發中的PK/PD引導:在I/II期臨床試驗中,密集采集PK和PD數據,建立群體PK/PD模型。該模型能定量描述劑量-暴露-效應-安全性的關系,用于支持后續試驗的劑量選擇、特殊人群(如肝腎功能不全者)給藥方案調整以及支持注冊上市。
- 免疫原性風險評估與管理:從分子設計階段就考慮降低免疫原性風險(如人源化、去免疫原性設計)。建立貫穿臨床前和臨床階段的靈敏檢測方法,評估抗藥物抗體的發生率、滴度、中和能力及其對PK、PD和安全性的臨床影響。
結論:
生物技術產品與大分子藥物的開發是一項系統工程,其核心驅動力在于對藥動學與藥效學相互作用的深刻理解和主動調控。從靶點選擇、分子設計、臨床前評價到臨床開發,PK/PD原則如同導航儀,指引著技術開發的方向。通過整合現代生物工程技術、分析方法和建模模擬工具,不斷優化藥物的暴露-效應關系,是提高開發成功率、最終為患者帶來更優治療選擇的關鍵所在。隨著細胞與基因療法等更復雜生物制品的涌現,對其獨特的體內命運和作用機制的PK/PD研究將變得更為重要和富有挑戰性。
如若轉載,請注明出處:http://www.pz900.cn/product/38.html
更新時間:2026-01-05 02:15:54